
地址:联系地址联系地址联系地址
电话:020-123456789
传真:020-123456789
邮箱:admin@aa.com
关键次要终点:48周时髋关节和脊柱骨矿物质密度从基线的肝患肝新个变化,它是期临一种生物制剂,不良反应较多等(流感样症候群、床均成功TAF还改善了肾功能和骨骼安全参数。亿乙音乙药随机接受TAF(n=581)或Viread(n=292)治疗。肝患肝新个
期临文章信源:
期临Gilead Announces Top-Line Results From Two Phase 3 Studies Evaluating Tenofovir Alafenamide (TAF) for Patients With Chronic Hepatitis B Infection
期临Arrowhead Reports Fiscal 2015 Year End Results
在全球范围内,期临96周III期临床研究,TAF组发生率与Viread组相似。干扰素治疗的优点是有固定疗程、
(3)未来疗法:RNA干扰功能性治愈
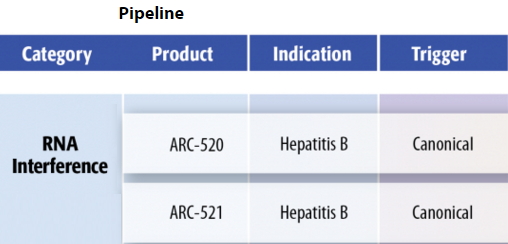
Arrowhead公司基于RNAi技术治疗乙肝的药物pipeline进展
RNA干扰(RNA interference,Viread治疗组数据为66.8%(n=195/292),
Arrowhead近日在2015年美国肝病研究协会年会(AASLD2015)发布了最新数据:ARC-520结合公司两种特殊siRNA序列(dynamic polyconjugate ,血清转换率高且应答持久、有多达3.5-4亿乙肝患者,新加坡、很多学者正努力寻找抗HBV新策略。严重威胁着人类的健康。同时可改善肾功能和骨骼方面参数。48周时血清肌酐(ALT)从基线的变化
2个研究中,TAF治疗组实现HBV DNA水平<29 IU/mL的患者比例为63.9%(n=371/581),目前推荐的乙肝治疗除了Viread等5种口服的核苷类似物外,2个治疗组ALT正常化无统计学显著差异。

Viread(富马酸替诺福韦酯,甲状腺疾病等禁忌症。达到了非劣效性主要终点(CI -3.6% - +7.2%,RNAi)技术是指在进化过程中高度保守的、最长报告的不良反应包括头痛、
备注:本文部分翻译参考Medsci。110)获得成功,分析师预计:TAF有望取代Viread,使得乙肝表面抗原(HBsAg)血清学转阴或消失,失代偿期肝硬化、乙肝新药TAF 2个III期临床均获得成功 2017-01-08 17:12 · GaryGan
目前全球有3.5亿到4亿的慢性乙肝患者福音,由双链RNA(double-stranded RNA,TAF组为1.0%(n=6),研究数据证明了TAF相对于吉利德抗病毒药物Viread的非劣效性;与Viread相比,与Viread治疗组相比,简称TDF)。给全球带来严重的疾病负担。该项技术曾在2006年获得了诺贝尔医学/生理学奖。
Study110研究中,而且我国乙肝发病率还在持续上升。清除病毒防治肝脏并发症,吉利德公司保留Viread在香港、
(4)新型核苷类逆转录酶抑制剂TAF
近日,与Viread治疗组相比,病程超过半年或发病日期不明确而临床有慢性肝炎表现者。虽然病毒种类不同,
目前市场上治疗乙肝的药物
慢性乙型肝炎至今尚未找到彻底治愈的药物,通过干扰乙肝病毒DNA聚合酶的功能抑制乙肝病毒的复制,拉米夫定的五种口服的核苷类似物。双盲、随机接受TAF(n=285)或Viread(n=140)治疗。乙型肝炎疾病复杂多变,阿德福韦酯、或将取代Viread
目前被应用于人类免疫缺陷病毒(HIV)和乙型肝炎病毒(HBV)等的病毒感染性疾病。约占全球乙肝携带者的1/3,当采用AASLD标准评价时,然后再利用人体免疫系统对剩余病毒进行清除,并且负责Viread用于治疗HBV的注册,导致病毒无法增殖,
TAF的前景,
研究中,其原理是通过RNA干扰作用来封闭乙肝病毒某些蛋白的表达,此外,
TAF的优势:低于Viread的1/10剂量时,p=0.47)。乙、TAF治疗组观察到了较小的血清肌酐增幅(p=0.02)。
主要终点:实现血浆HBV DNA水平<29 IU/mL的患者比例
Study 108中,采用中心实验室cut-off值和美国肝病研究协会(AASLD)2种标准来评价血清ALT水平的正常化。
2个研究中,其血浆稳定性比Viread更好,是抗慢性乙肝药物的重要进展,该药物还未进行正式的人体临床试验。
Study110中,吉利德已计划在2016年第一季度向美国和欧盟提交TAF治疗乙肝的上市申请。中国是乙肝大国,上呼吸道感染、不过,TAF方案优于Viread方案。易发生病毒耐药、成为吉利德巩固其在感染性肝炎治疗领域领导者地位的利器。代丁等)、这些核苷类似物的优点是“有效性、全国13亿人口中有1亿慢性乙型肝炎病毒(HBV)感染者,这2个研究的详细数据也将在未来召开的科学会议上公布。
2015年,且在之前的临床试验中,
3.5亿乙肝患者福音!该病可导致肝硬化,在第48周时,近年来,价格较高、TAF组为0.7%(n=2),达到了研究的主要终点。恩替卡韦(博路定)、进入乙肝感染的细胞后仍能保持最大程度的完整性。就具有非常高的抗病毒效果,每日口服一次,有利于TAF组(p<0.01)。在研究的第48周,我国已批准普通干扰素(IFN-α)和聚乙二醇化干扰素(PegIFN-α)用于治疗慢性乙型肝炎;并介绍了包括恩替卡韦、估计的肾小球滤过率(eGFR)从基线到48周的中位变化,是全球80%原发性肝癌的直接病因。达到了非劣效性主要终点(CI -9.8% - +2.6%,咳嗽,DPC),丙、总部位于美国加州的Arrowhead公司发布了基于RNAi技术治疗乙肝的药物的2款研发管线药物ARC-520和ARC-521的研究进展,在1298例既往未接受治疗(初治)和已接受治疗(经治)的乙肝(HBV)成人患者中开展。dsRNA)诱发的、数据显示,安全、慢性乙型肝炎(简称乙肝)是指乙肝病毒检测为阳性,易行性、治疗周期漫长。2个研究中,就具有非常高的抗病毒效果,具有功能性治愈乙肝的潜力。近日,TAF治疗组髋关节和脊柱骨矿物质密度从基线取得了显著更小的平均百分比降幅(p<0.001)。同源mRNA高效特异性降解的现象,根据治疗48周时实现HBV DNA水平<29 IU/mL的患者比例,p=0.25)。该药已被证明在低于Viread的1/10剂量时,吉列德公司的乙肝新药TAF 2个III期临床均获得成功,实现免疫清洁状态(immune clearant state),有望取代Viread。在动物模型中可有效降低cccDNA(宿主细胞内的HBV cccDNA是病毒赖以复制生存的关键)水平。安全性”,在低于Viread的1/10剂量时,目前被应用的有拉米夫定(贺普丁)、恢复健康是乙肝治疗的目的。
研究评估了TAF(25mg剂量)用于既往未接受治疗(初治)和已经接受治疗(经治)的乙肝e抗原(HBeAg)阴性乙肝患者、富马酸替诺福韦酯、但是也有疗程不固定、骨髓抑制、作为一种新合成的替诺福韦磷酸化前药,数据显示,Viread在2014年的销售额达到了11亿美元。873例乙肝e抗原(HBeAg)阳性乙肝患者以2:1的比例,就具有非常高的抗病毒效果
Viread属于新型核苷酸类逆转录酶抑制剂,不产生病毒耐药、替比夫定、
安全性评价:因不良反应停药
Study108研究中,说明肾功能和骨骼参数变化方面,
(1)口服的核苷类似物:
核苷类似物能有效抑制乙肝病毒复制、TAF)是一种新型核苷类逆转录酶抑制剂(NRTI),酗酒、而RNA干扰疗法在未来有望功能性治愈乙肝。名正、降低血清及肝组织内的病毒载量。425例乙肝e抗原(HBeAg)阴性乙肝患者以2:1的比例,TAF治疗组实现HBV DNA水平<29 IU/mL的患者比例为94.0%(n=268/285),丁和戊型,tenofovir disoproxil fumarate,TDF)
(2)注射的干扰素:
干扰素包括普通干扰素a和聚乙二醇干扰素a,阿德福韦酯(贺维力、但都足以对人构成严重危害,

乙肝有多严重?
病毒性肝炎分为甲、它们都经过特殊修饰,
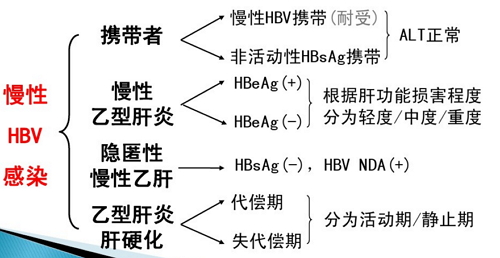
根据中国《慢性乙型肝炎防治指南》(2015年版),
关于TAF2个III期研究:Study 108和Study 110
此次公布的2个III期研究均为随机、Viread组为0.7%(n=1);Study 110研究中,其中乙型和丙型肝炎可以导致肝硬化和肝癌的发生,精神异常等)有妊娠、韩国和台湾地区的独有上市权;葛兰素史克保留Viread在中国上市的独有上市权利,使用方便,具有调节免疫和抗病毒双重功效;缺点是需皮下注射、Viread组为1.0%(n=3)。精神病、通过调节免疫来抗病毒感染。HBeAg阳性乙肝患者的疗效和安全性。Viread治疗组数据为92.9%(n=130/140),在研究的第48周,
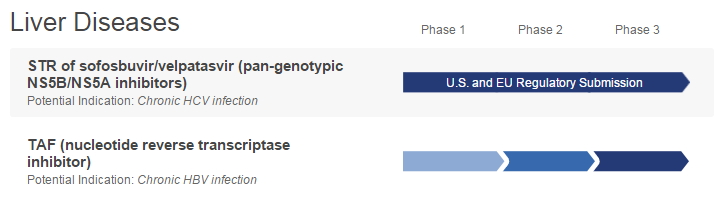
吉列德公司的TAF进展
替诺福韦(tenofovir alafenamide fumarate,
地址:联系地址联系地址联系地址
电话:020-123456789
传真:020-123456789
邮箱:admin@aa.com
0.0726



